Хто такий містер CRISPR?
5 Червня 2016 | IgorZinchuk
Категорія: Біологія
Теги: CRISPR, генетична інженерія, генна терапія, молекулярна біологія
1985. Виходить номер журналу Science під номером 230 зі статтею “Enzymatic amplification of beta-globin genomic sequences and restriction site analysis for diagnosis of sickle cell anemia” за авторством Кері Мулліса. Саме тоді і відбулась революція у генній інженерії. Полімеразна ланцюгова реакція дала можливість вченим в усьому світі проводити генні досліди без думки про нестачу досліджуваного матеріалу.
2012. Американський генетик Брюс Конклін працює над своєю дипломною роботою. Він хоче внести зміну лише в один ген, та, на жаль, технології, якими він користується, занадто незручні та дорогі. Випадково він натикається на публікацію про новітній метод CRISPR. Цей метод обіцяє швидке і дешеве редагування геному будь-якого створіння, включаючи людину. І грянув грім. Почалась ера “CRISPR лихоманки”.
2013-2015. Editas Medicine:CRISPR терапія (43 мільйонів доларів), INTELLA THERAPEUTICS:CRISPR терапія (15 мільйонів доларів), CRISPR THERAPEUTICS:CRISPR терапія (89 мільйонів доларів).
2015. Звичайного квітневого дня стрічки профільних та не дуже новин гуділи він однієї новини: ”Вчені модифікували ембріон людини за допомогою CRISPR”. І саме тоді з’явились перші етичні питання цього відкриття.
Увага!Attention! Стаття наповнена відсилками, сленгом та інтернет мємєсами(Єєєє,рокккккккк)!
Цинкові пальці?
Насправді вчені вже могли редагувати геном і досить успішно, але є одне але, як казав Майкл Щур. 5000$ хрумких американських доларів за мінімальний набір ендонуклеаз моделі “цинкові пальці”. Але до своєї новенької і блискучої ендонуклеази (фермент, що розщеплює нуклеїнові кислоти зсередини їх послідовності) потрібно прикупити добрячий “гараж” у вигляді специфічних реагентів для зберігання, оновлення деталей твоєї новенької іграшки (все ламається і це теж) та багато чого цікавого. Ще накинь наверх складність у виробництві “цинкових пальців” і ти маєш такий собі Ролс Ройс у світі молекулярних ферментів для вчених.
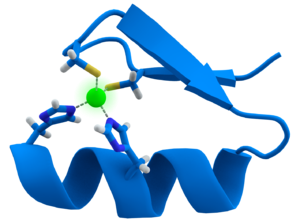
Власне ці «цинкові пальці». Автор зображення Thomas Splettstoesser (власна робота), розповсюджено на умовах http://www.gnu.org/copyleft/fdl.html чи CC BY-SA
Здавалось би, у чому проблема? Інструмент є, живіть собі і користуйтесь ним. Та все змінила E. coli (кишкова паличка, бактерія). Мені завжди було цікаво, а як захищаються бактерії від вірусів? Вам теж? Зараз спробую на пальцях пояснити. Запускаємо нашу Делоріан і вперед у минуле, док!
Імунна система бактерій
…планета Земля. Навколо — неосяжні простори води, повітря та ґрунту, що кишать твоїми конкурентами. Варто тобі відзначитися від сусіда справа мутацією всього в одному важливому гені, яка не дасть тобі переробляти органіку так само добре, як йому, і все, твоя еволюційна гонка програна, манускрипт твого генома забутий і її викреслять із історії генофонду прокаріот… Та не хвилюйся, маленький прокаріот, в тебе є CRISPR/Cas (нудна розшифровка абревіатури: з англ. – короткі паліндромні повтори, регулярно розташовані групами / CRISPR-асоційовані білки)!
Це прямі повтори та унікальні послідовності в ДНК бактерій і архей, які спільно з асоційованими генами (Cas, англ. CRISPR-associated genes) забезпечують захист клітини від чужорідних генетичних елементів (бактеріофагів, плазмід). Повтори розділені спейсерами. Спейсери за своєю нуклеотидною послідовностю відповідають певним фрагментам ДНК чужорідних генетичних елементів (бактеріофагам, плазмід). У зв’язку з цим було запропоновано і потім доведено, що послідовності нуклеотидів, які розділяють повтори, походять від послідовностей геномів бактеріофагів, і, відповідно, забезпечують захист клітин від інфекцій (Хвала Вікіпедії!).
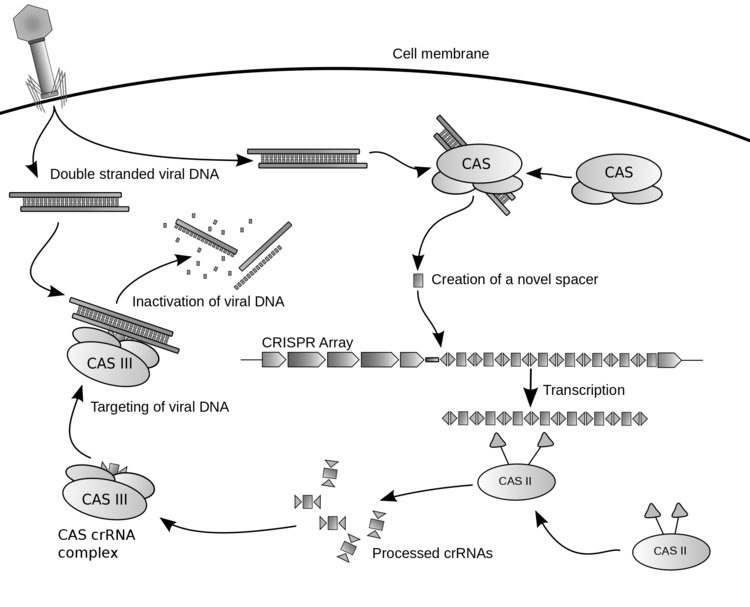
Робота CRISPR. Автор зображення James atmos (власна робота), розповсюджено на умовах CC BY-SA 3.0
І от, в 1987 році група вчених знаходить у E.coli цей механізм. 1995 року встановлено загальність цих повторів у багатьох мікроорганізмів. 2007 вчені харчової компанії Danisko доводять, що це система захисту бактерій, і у 2011 перше комерційне направлення у вивченні CARIBOU SCIENCE виділяє на це 11 мільйонів доларів.
Ви зараз мабуть думаєте: “Цей чувак вже довго нам щось каже про те, що це революція та не пояснив чому”. Не хвилюйтеся, ми вже майже дійшли до розв’язки нашої гостросюжетної генетичної повісті.
30$
Що можна купити за 750 гривень або 30$? Наприклад, порцію м’яса алігатора або Цитрус Кумкват. Або купити виборця, як роблять деякі депутати.
Але це все дурня. Я дам вам за ці гроші інструмент Бога. Я дам вам CRISPR.
Методологія CRISPR швидко затьмарила собою нуклеази “цинкові пальці” та інші інструменти для редагування. Для декого це означає відмову від технік, на які були витрачені роки для їх поліпшення. “Я пригнічений”, — каже Білл Скарнес, генетик з Хінкстон (Великобританія), — “але в той же час схвильований”. Скарнес витратив чималу частину своєї кар’єри, використовуючи технологію, впроваджену в середині 1980-х: вбудовування ДНК в ембріональні стовбурові клітини і подальше використання цих клітин для створення генетично модифікованих мишей. Техніка стала в лабораторії головною, але вона також була трудомісткою і дорогою. CRISPR вимагає набагато менше часу, і, урешті-решт, Скарнес прийняв цю технологію два роки тому.
 Раніше, якщо ти хотів подивитись як спрацює твоє генне редагування, ти мав скористатись послугами дрозофіл чи мишей (просто на них простіше було відслідкувати зміни). Що зробив CRISPR? Він дав тобі набір фарб, а світ живих організмів перетворив на полотно. Мишки, які світяться, — легко! Лікування генетичних хвороб (привіт міопатія Дюшена і т.д.)? — Просто! Зробити нові сорти агрокультур для більшого урожаю і з кращим смаком? — Тільки попроси. Контролювати популяцію малярійних комарів? — І це ми можемо. Зробити дріжджі, які будуть продукувати опій (ліки)? — Простіше простого, мій маленький англієць-колоніст Китаю! І все це лише за 30$!
Раніше, якщо ти хотів подивитись як спрацює твоє генне редагування, ти мав скористатись послугами дрозофіл чи мишей (просто на них простіше було відслідкувати зміни). Що зробив CRISPR? Він дав тобі набір фарб, а світ живих організмів перетворив на полотно. Мишки, які світяться, — легко! Лікування генетичних хвороб (привіт міопатія Дюшена і т.д.)? — Просто! Зробити нові сорти агрокультур для більшого урожаю і з кращим смаком? — Тільки попроси. Контролювати популяцію малярійних комарів? — І це ми можемо. Зробити дріжджі, які будуть продукувати опій (ліки)? — Простіше простого, мій маленький англієць-колоніст Китаю! І все це лише за 30$!
Хоча, як і будь-яка технологія, CRISPR має недоліки. Сучасна модель CRISPR під назвою Cas9 має достатній відсоток похибки, щоб утримувати вчених від широкого використання його у лікуванні генетичних хвороб. Плюс, єдиним на даний момент способом доставити CRISPR у клітини є вірус, а вірусів деякі вчені бояться і тікають від них, як від вогню. І закони, що випускають у прогресивних країнах, обмежують дослідження… Та не все так погано! Точність Cas9 виправлять її заміною на Cpf1, а віруси використовують контрольовані і які ми добре розуміємо, а із законами нам допоможуть Докінз та настанови Сагана.
Див. також Де не справляється людська – справиться бактеріальна імунна система
Де не справляється людська – справиться бактеріальна імунна система: Можливості застосування CRISPR/Cas9 для генної терапії вірусу імунодефіциту людини (кінець)





Обговорення