Чим більше опір, тим більше сили
або Один із прикладів пристосувального сигнального значення вільних радикалів
«Для чого нам потрібне Серце?»
«Для того, щоб дихати і кохати»
Олександр, 4 роки.
Людина все своє життя опирається труднощам і негараздам, щоб іти вперед. Відступає, спочиває – і знову в бій. Але серце перемагає опір крові кожну секунду і не має жодної миті на перепочинок. Кардіологи більш як сто років вивчали, як це йому вдається. Нещодавно виявилося, що серцю у цій непростій боротьбі допомагають вільні радикали.
У 1912 році молодий хлопець на ім’я Гліб Анреп, студент 2-го курсу Санкт-Петербурзької Військово-медичної академії за рекомендацією Івана Петровича Павлова поїхав до Лондону. І не куди-небудь, а до лабораторії, в якій сумлінно займалися фізіологічними дослідженнями видатні фізіологи Ернст Старлінг і Вільям Бейліс. Студент дуже вдало долучився до пізнання дивовижних подій, що відбуваються у серці. Відкриття, яке так натхненно та влучно зробив хлопець того ж року, вже понад століття носить його ім’я – ефект Анрепа. Суть цього ефекту полягає в тому, що серце починає скорочуватися сильніше при збільшенні тиску крові в аорті.
Гліб Анреп встановив, що в кінці скорочення лівого шлуночка, коли кров викидається до аорти і створює там все вищий тиск, м’язового напруження стінок шлуночку стає недостатньо для продовження витискання крові в аорту. Тому крові з серця виходить менше, що мало б знизити кровопостачання організму. Проте через лічені мілісекунди ситуація виправляється: міокард напружується і долає опір аорти. Як же клітини серця (кардіоміоцити) «знають», що саме зараз треба пересилити тиск крові й зберегти кількісні показники – ударний і хвилинний об’єм крові – на потрібному рівні?
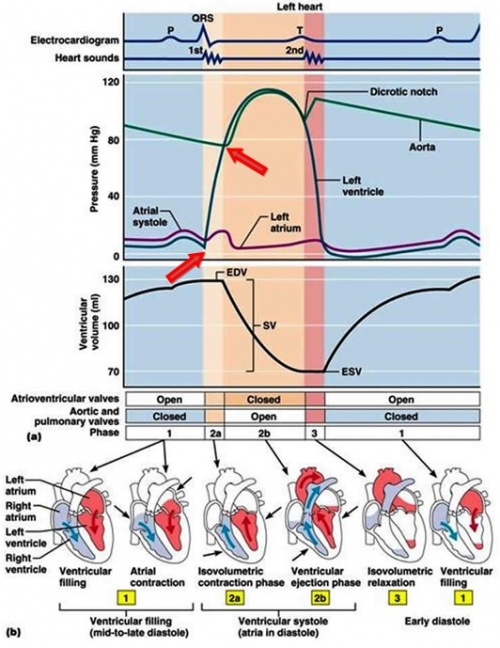
Подальші дослідження ефекту Анрепа були продовжені самим Ернстом Старлінгом і багатьма іншими відомими фізіологами. Пізніше вчені назвали це «гомеометричним механізмом» (без зміни розміру камер серця) регуляції діяльності серця, сенс якого полягає у забезпеченні адекватного хвилинного об’єму крові за будь-яких умов, наприклад при виконанні фізичного навантаження. Дослідники, які намагалися пояснити механізми такого збільшення сили назвали його «феноменом», адже кожна запропонована версія ставила більше запитань, ніж давала відповідей.
І ось, нарешті, майже сто років потому ми можемо сказати, що феномен перестає бути загадкою. Вийшли узагальнюючі роботи на кшталт «The Anrep effect: 100 years later», яка була надрукована на початку 2013 року у журналі American Journal of Physiology — Heart and Circulatory Physiology, де з окремих досліджень було зібрано картину молекулярно-біохімічних подій, які відбуваються в кожній клітині серця, починаючи від збільшення тривалості напруження серцевого м’яза без зміни довжини (так зване ізометричне скорочення) до збільшення сили його скорочення.
У нормальних умовах серце виштовхує кров до аорти при тиску в ній близько 80 мм.рт.ст. (так званий діастолічний тиск, після розслаблення шлуночків серця). Коли ж в аорті зростає тиск, скажімо, з 80 мм.рт.ст. до 100 мм.рт.ст. (післянавантаження на серце), зростає і час,необхідний для досягнення цієї величини тиску в шлуночку. Ясно, що інакше кров зі шлуночка в судини просто не надійде, оскільки рух крові, як і будь-якої рідини, забезпечується різницею тисків: з об’єму з вищим тиском до об’єму з нижчим. У цей час, а саме фази ізометричного скорочення серцевого циклу, зростаєнапруження еластичних регіонів молекули тітіну, до якої кріпляться актинові і міозинові філаменти.
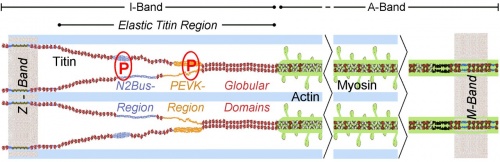
Ці механічні зміни активують низку протеїн-кіназ, які фосфорилюють білки кардіоміоцитів, що здійснюють екзоцитоз. З везикул назовні виходять гранули з ангіотензином II та ендотеліном – біологічно активними речовинами. До цих молекул на клітинах серця є мінералокортикоїдні рецептори й рецептори епідермального фактору росту. Активовані рецептори запускають каскад подій, що починається з фосфорилювання NADPH-оксидази 4 (NOX4) – ферменту, який збільшує рівень вільних радикалів в клітині. На збільшення кількості радикалів реагують спеціальні редокс-чутливікінази, однією з задач яких є активація Na+/H+ обміннику (NHE1) клітинної мембрани. Цей насос виганяє з кардіоміоциту іони водню, натомість запускає всередину іони Na+. Коли натрію в клітині багато, то це, звісно, ненормально. Навіть натрій-кальцієвий насос, основною метою якого є виведення кальцію з кардіоміоциту, в таких умовах стає воротами для вхідного кальцієвого струму і несе кальцій всередину клітини. І тут клітина досягає необхідної умови для розвинення більшої сили – вона збільшила концентрацію Ca2+ в своїй цитоплазмі! Оскільки разом цих кардіоміоцитів багато, разом вони стають сильніше і можуть подолати опір, а отже виконати своє призначення – виштовхнути потрібний об’єм крові до аорти!
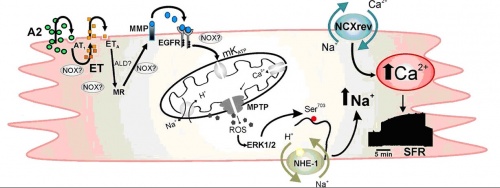
Ми бачимо, що маленький кардіоміоцит вже має запрограмовані ендогенні механізми спротиву збільшенню зовнішнього тиску і залучає сусідні клітинки у важливу справу. Залишається побажати всім нам успішної реалізації власних можливостей і запрограмованих механізмів спротиву і збільшення сили духу для спільного подолання зовнішнього тиску 🙂
Тетяна Древицька
The Anrep effect: 100 years later
Horacio E. Cingolani , Néstor G. Pérez , Oscar H. Cingolani , Irene L. Ennis
The Giant Protein Titin as an Integrator of Myocyte Signaling Pathways
Wolfgang A. Linke, Martina Krüger





Обговорення
23 Березня 2017, 21:13
ok
Напишіть відгук