Епігенетична «дієта»: без гіпоксії ніяк
7 Грудня 2014 | TetjanaDrevytska
Категорія: Медицина
Теги: HIF, гіпоксія, епігенетика, метилювання, ожиріння, целюліт
Немає нічого дивного в тому, що причини, механізми розвитку та методи корекції такої поширеної патології як ожиріння цікавлять багатьох. За даними ВООЗ:
- з 1980 року кількість людей, які страждають ожирінням, у світі зросла більше ніж вдвічі
- більш як 1,4 мільярди дорослих людей у віці від 20-ти років страждають від надлишкової ваги (це взагалі жахливі цифри, вдумайтесь – це 20% населення Землі!). З них більше 200 мільйонів осіб чоловічої та майже 300 мільйонів жіночої статі страждають на ожиріння
- у 2012 році більше 40 мільйонів дітей у віці до 5 років мали надлишкову вагу або ожиріння
А чи можна запобігати ожирінню?
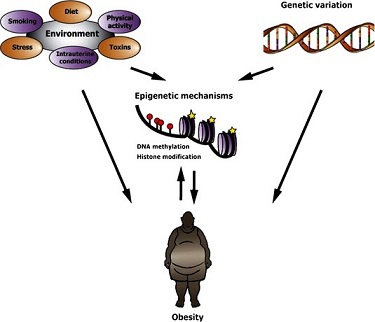
Наукова стаття, яка випадково потрапила на очі автору, є прикладом розвитку нового напряму сучасної науки – проекту під назвою «Епігеном». Дослідники вивчали епігенетичні (ви ж читали попередні статті «Моєї науки»? цю і цю) зміни, а саме рівень метилювання ДНК цілого ряду генів у хворих на ожиріння та людей з підвищеним індексом маси тіла (ІМТ). Треба сказати, що зв’язок між певними варіаціями ряду генів, (які містили близько 30 так званих однонуклеотидних поліморфізмів, SNP) та ІМТ вже був установлений раніше. Тепер стало ясно, що ожиріння має спадковий компонент. Тим часом, мало було відомо про епігенетичні зміни, пов’язані з ІМТ. У новій роботі автори провели пошук асоціацій між рівнем метилювання трьох ділянок гену HIF-3α (hypoxia induced factor – фактор, який індукується гіпоксією) та ожирінням.* Вони встановили, що збільшення ІМТ у дорослих людей європейського походження пов’язане з підвищеним рівня метилювання певних ділянок гену HIF-3α у клітинах крові та в жировій тканині.
* Нагадаємо читачам – чим вищій рівень метилювання гену, чи певних його регуляторних ділянок, тим нижче рівень його експресії, менше кінцевого продукту – білку.
Далі ми можемо розмірковувати – таке підвищення рівня метилювання є наслідком чи причиною розвитку ожиріння? Для того, щоб відповісти на це запитання, необхідно дослідити роль транскрипційного фактору HIF у розвитку ожиріння і взагалі згадати, що то за фактор такий.
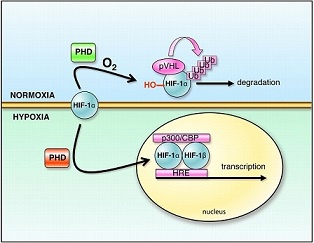
Зазвичай згадують про роль HIF при зменшенні кількості кисню, що надходить до клітин під час нормального розвитку або при патологічних процесах (наприклад, при серцево-судинних захворюваннях і пухлинах). Він є транкрипційним фактором і після отримання відповідного сигналу, як то зниження парціального тиску кисню в клітині або підвищення рівня вільних радикалів (тут трошки про те, як вони можуть бути нам корисними) зв’язується зі своїми компаньонами і транспортується в ядро. В ядрі HIF знаходить спеціальні послідовності в промоторах генів. Такі послідовності називають елементи відповіді гіпоксії (англійською це звучить Hypoxia-Response Element — HRE і виглядає так: 5′-ACGTG-3′). Всі гени, які мають таку консервативну послідовність називають генами-мішенями HIF і їх надзвичайно багато.
Останнім часом збільшилась кількість експериментальних даних щодо участі системи HIF в обміні речовин, регуляції витрат енергії та розвитку ожиріння. Більш того, деякі вчені стверджують, що цьому фактору належить ключова роль у регуляції системного метаболізму та ваги тіла. Зокрема є одна робота, у якій показано, що порушення роботи HIF-1α або ARNT (HIF-1β) у адипоцитах (жирових клітинах) пов’язане зі зменшенням утворення жиру, захистом від ожиріння і інсулінорезистентності. Також вчені виявили, що «вимкнення» гену HIF-1α за допомогою коротких антизмістових молекул ДНК протягом 8 тижнів у мишей з висококалорійною дієтою істотно збільшує витрати енергії і стимулює втрату ваги.
А от про субодиницю HIF-3α відомо, що вона є негативним регулятором субодиниці 1α. Це є беззаперечним фактом, який підтверджено у декількох лабораторіях світу і в нашій також. Тобто, якщо субодиниці HIF-3α синтезується багато – всі мають худнути, ставати стрункими та тендітними?) Виходить, що так! І збільшення рівня метилювання цього гена (а значить, і зменшення його кінцевого продукту – білку) дійсно має призводити до збільшення індексу маси тіла! І є його причиною, а не наслідком!

Все було б ясним і зрозумілим, як би не ось це запитання: а де ви бачили товстих спортсменів? Звісно, мова не йде про традиційне японське бойове мистецтво, а от серед бігунів чи плавців бачили? Я – ні.
Чому мова зайшла саме про плавців? А справа у тому, що кілька років тому у нашій лабораторії ми проводили дослідження на щурах із використанням такого виду фізичного навантаження, як плавання. Вийшли треновані спортсмени: авжеж – наші тварини плавали кожного дня цілий місяць! Половині щурів ми двічі вводили малі інтерференційні РНК (siRNA) до гену HIF-3α. Таким чином ми добились зниження рівня матричної РНК, яка кодує цей білок, у 2,5 рази. Що ж ми мали побачити? Кволих, товстих і нездатних до спортивних досягнень тваринок. Нічого подібного! Наші треновані щури, яким був введений такий «генетичний допінг», мало того що були стрункими, жвавими і зацікавленими у всьому, що відбувалося навкруги, а ще й ставили рекорди з плавання! У цілому вони плавали з вантажем до відмови на 40% довше, ніж треновані без інтерферующих РНК щури. Хм, там де мова йде про десяті і соті секунди, на 40% краще, ніж опоненти — це просто космос!
Ну і ще одна дослідницька робота, що допомагає нахилити ваги в інший бік від позначки «причина»…
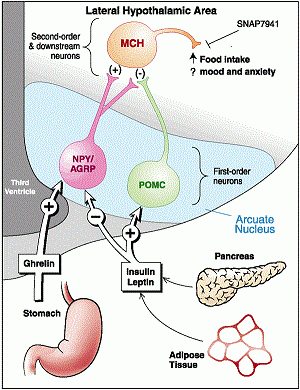
Автори цього дослідження вивчали роль центральної нервової системи у регуляції маси тіла. Гіпоталамус є головним регулятором споживання їжі, утворення та витрат енергії. А маса тіла є результатом балансу між споживанням та витратами. Нейрони гіпоталамусу не лише визначають рівень таких молекул, як лептин, грелін та інсулін, а ще й зондують кількість поживних речовин – глюкози, амінокислот, жирних кислот. Проопіомелатокортин (ПОМК) – ключовий білок, який бере участь у визначенні рівня глюкози. Утворюється він у спеціальних клітинах, так званих ПОМК-нейронах.
Дослідники показали, що, по-перше, ПОМК синтезується тільки за командою HIF (це ж фактор транскрипції, не забули?), а по-друге, якщо в ПОМК-нейронах експериментально викликати нестачу HIF-1α, спостерігається зниження чутливості до глюкози, не пригнічується активність нейронів у центрі голоду в гіпоталамусі, з’являються прояви енергетичного дисбалансу та розвивається ожиріння.
Так що, збільшення рівню метилювання HIF-3α – це наслідок ожиріння? Хочете, ми замінимо це на компенсацію? Мені так навіть більше подобається.
Тобто, за цею логікою, першопричиною була недостатньо активна робота транскрипційного фактору HIF-1α, що призводить до підвищення ІМТ, розвитку ожиріння тощо. І тепер зрозуміло, що саме треба зробити організму: заблокувати негативний регулятор HIF-1α! Що з успіхом досягається підвищенням рівня метилювання цього регулятора. Звичайно, а як же ще компенсувати?
Відомо, що HIF-1α та HIF-2α активують розщеплення жирів (ліполіз). Рівень жирних кислот у людей, хворих на ожиріння, підвищується. А що робити? Чим замінити глюкозу, яка не може потрапити в клітини через інсулінорезистентність?
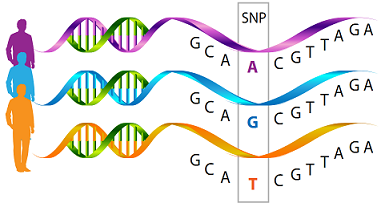
Такі варіації поодиноких нуклеотидів в генах відповідають за те, що ми маємо різний колір очей, різні уподобання та різні схильності.І наостанок, не можу не згадати про одну генетичну цікавинку – вже знайомі вам алельні поліморфізми генів, або генетичні варіації, але стосовно такої «косметичної» проблеми, як целюліт. Так вийшло, що розвиток, або краще сказати ризик розвитку, целюліту у представниць чарівної статі тісно пов’язаний із тією генетичною варіацією гена HIF-1α, яку ми почали прицільно вивчати роки тому (можна ознайомитись із коротним вмістом робіт: перша і друга). Так от, наявність в геномі рідкісного алелю Т/С суттєво знижує і ризик розвитку, і ступінь прояву целюліту. Ген з Т алелем експресується краще, а білок, зчитаний з такого гена, живе довше. А що ж робити тим, кому не так пощастило (по правді сказати, алель Т не так часто зустрічається у нашій, українській популяції), і вони є носієм так званого алелю «дикого типу» — більш поширеного? Очевидно! Це ж фактор, що індукується гіпоксією і треба його тренувати! – регулярно: гори, пірнання, помірне фізичне навантаження, просто періодична затримка дихання.
Або ще простіше: коли ми затамовуємо подих від подиву, від задоволення, від щастя… така періодична гіпоксія – найкращі ліки від усього!
Посилання
DNA methylation and body-mass index: a genome-wide analysis. Katherine J Dick, Christopher P Nelson et al.
Role of hypoxia in obesity-induced disorders of glucose and lipid metabolism in adipose tissue. Jun Yin, Zhanguo Gao et al.
HYPOXIA AND ADIPOSE TISSUE FUNCTION AND DYSFUNCTION IN OBESITY. Paul Trayhurn





Обговорення